在抗癌道路上,我们始终怀揣期待,盼望着新型抗癌药物能不断涌现,为战胜癌症提供更强大的武器和更多样的选择。
2024年5月9日,新型PD-L1抑制剂——贝莫苏拜单抗,经过严格的审核与评估,正式获得了中国国家药品监督管理局(NMPA)的批准。贝莫苏拜单抗联合盐酸安罗替尼胶囊及化疗(注射用卡铂、依托泊苷注射液),为初诊为广泛期小细胞肺癌(ES-SCLC)的患者,铺就了一条全新的治疗道路,为他们带来了更多的选择与希望。
一、 贝莫苏拜单抗“新”升级,助力抗癌长征途
贝莫苏拜单抗是新型人源化IgG1亚型PD-L1抑制剂,可以直接作用于肿瘤细胞的表面的PD-L1受体,阻止肿瘤细胞产生免疫逃逸,重新激活免疫细胞对肿瘤的杀伤作用。
机制强化:作为一款PD-L1抑制剂,贝莫苏拜单抗可以有效阻止PD-L1与T细胞表面PD-1和B7.1的结合,有助于全面激活T细胞的抗肿瘤功能;与此同时,贝莫苏拜单抗不阻断PD-L2通路,因此可以保留自身免疫调节功能,降低免疫相关不良反应(irAE)的风险[1-3]。
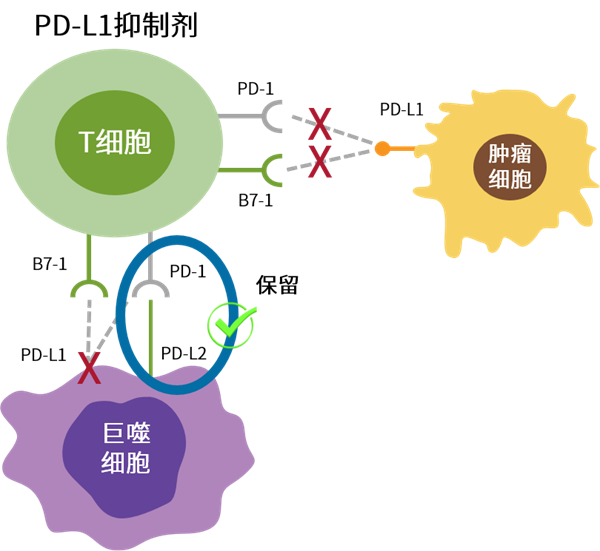
结构创新:贝莫苏拜单抗是采用IgG1亚型并进行Fc段改造的新型PD-L1抑制剂。
IgG1是血清和体液中含量最高的抗体,具有结构稳定,高亲和力的特点,与PD-L1蛋白结合力强,能够高效阻断PD-L1/PD-1信号通路;但是天然的IgG1具有较强的Fc效应,可能会引发过度的免疫反应,从而导致不可控的疗效损失和irAE[4,5]。
因此,贝莫苏拜单抗在Fc段定点改造,去除抗体依赖的细胞介导的细胞毒性作用(ADCC)及补体依赖细胞毒性作用(CDC),减少免疫相关细胞损耗,避免Fc效应对免疫细胞的误伤或错杀,最大限度的释放贝莫苏拜单抗的抗肿瘤活性,降低irAE的发生风险。
同时,人源化(即抗体在结构和功能上与人体自身产生的抗体非常相似)的设计特点进一步保证了IgG1亚型抗体抗击肿瘤的稳定性,减少了患者体内可能产生的免疫反应[6,7]。
二、“四重奏”联合“新”方案,唱响生命交响曲
联合疗法是指将两种或多种药物,同时或交替使用,以期达到协同或加成的效果,或者减少不良反应的一种治疗策略。
近几年,随着免疫联合化疗在ES-SCLC研究结果的推动,免疫联合化疗已经替代化疗成为ES-SCLC的一线治疗,尽管如此,免疫联合化疗在ES-SCLC的生存获益仍十分有限,中位总生存期(OS)徘徊在12-15.8个月,中位无进展生存期(PFS)仍然没有超过6个月,无法满足ES-SCLC患者迫切需要改善生存的需求[8-13]。
既往的临床前研究结果提示,有限的生存获益可能归因于小细胞肺癌复杂的肿瘤微环境,主要表现为免疫抑制、高血管生成及血管化[14]。基于此,预期免疫联合抗血管生成治疗,再结合标准化疗将有可能产生更为优异的效果。
研究者们这就探索出了一个新的联合疗法,即四药联合治疗方案:将贝莫苏拜单抗、安罗替尼、铂类药物和依托泊苷四种药物同时使用,作为SCLC的一线治疗。
从作用机制看,“四药联合”方案中,每种药物各司其职,但又互相协同:
贝莫苏拜单抗:抗PD-L1的单克隆抗体,可以阻断PD-L1与PD-1、B7.1结合,从而激活免疫系统,增强细胞毒性T细胞对肿瘤细胞杀伤功能。
安罗替尼:小分子多靶点酪氨酸激酶抑制剂,对肿瘤血管生成及肿瘤生长具有广泛的抑制作用;同时安罗替尼可以调节肿瘤免疫微环境,并通过联合PD-1/PD-L1抑制剂促进抗肿瘤免疫反应,联合免疫治疗协同增效[14,15]。
依托泊苷和卡铂:化疗药物,直接破坏肿瘤细胞的DNA,阻断其生长和繁殖 。
那么,问题来了,四药联合方案,是否带来令人欣喜的治疗结果呢?
三、攻坚克难“新”突破,研究数据显真章
ETER701研究给出了肯定的答案!这是一项随机、双盲、安慰剂对照的Ⅲ期临床研究,旨在探索贝莫苏拜单抗联合安罗替尼及化疗一线治疗ES-SCLC的疗效及安全性。2023年,该研究结果在世界肺癌大会(WCLC)一经报道,就引发了广泛的关注!
研究结果显示[16],接受贝莫苏拜单抗联合安罗替尼、卡铂和依托泊苷四药联合方案治疗的246例ES-SCLC患者,中位PFS和OS显著高于对照组,且刷新了历来的PFS和OS纪录!两组中位PFS分别为6.9个月 vs 4.2个月,两组中位OS分别为19.3个月 vs 11.9个月!
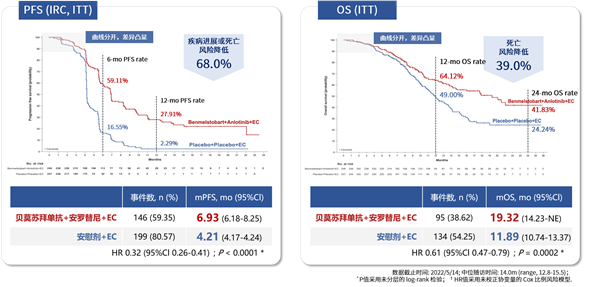
在关注患者用药体验的过程中,我们发现相较于对照组治疗方案,四药联合组三级及以上治疗相关不良事件(TRAEs)的发生率并无明显差异,更令人欣慰的是,在整个治疗过程中,并未观察到任何新的不良反应的出现[16]。这一发现不仅证明了四药联合治疗方案在不良反应方面较为可控可耐受,更意味着患者在接受此治疗时无需担心额外的风险。这种创新的多药联合方案,不仅为患者提供了更为全面的治疗选择,同时也让患者在治疗的道路上更加安心。
四、立足当下新选择,展望未来新篇章
贝莫苏拜单抗、安罗替尼与化疗药物的强强结合,为ES-SCLC患者的长期生存开辟了新的道路,带来了更多的可能与希望!这种四药联合的策略,为ES-SCLC一线治疗谱下了新的篇章,推动了小细胞肺癌治疗格局的改变,给万千肿瘤患者及家庭点亮了抗癌道路上的明灯!
小细胞肺癌这道医学难题,在医学研究与新药研发的不断探索中,正逐步显露新的突破。我们有理由深信,未来会有更多的创新方案涌现,助力患者走向康复。
在这个变化的时代,我们鼓励每位患者珍视当下的生活,细心感受身体的每一个变化,积极拥抱生活的每一个瞬间。严格遵循医生的指导,以积极的心态面对治疗,共同书写属于自己的生命传奇,迎接更加美好的明天!
参考文献:
1.Boussiotis VA. et al. N Engl J Med 2016; 375:1767-1778.
2.Chen DS, et al. Clin Cancer Res. 2012 Dec 15;18(24):6580-6587.
3.Pillai RN, Behera M, Owonikoko TK, et al. Cancer. 2018 Jan 15;124(2):271-277.
4.Chen Y, Pei Y, Luo J, Huang Z, et al. Front Immunol. 2020 May 29; 11:1088.
5.Keir ME, Butte MJ, Freeman GJ, Sharpe AH. Annu Rev Immunol. 2008; 26:677-704.
6.Buss NA, Henderson SJ, McFarlane M, et al. Curr Opin Pharmacol. 2012 Oct;12(5):615-22.
7.Shepard HM, Phillips GL, D Thanos C, et al. Clin Med (Lond). 2017 Jun;17(3):220-232.
8.Su Y, Luo B, Lu Y, Wang D, et al. Clin Cancer Res 15 February 2022; 28 (4): 793–809.
9.Liu S, Qin T, Liu Z, et al. Cell Death Dis 11, 309 (2020).
10.IMpower133: Horn L, Mansfield AS, et al. N Engl J Med. 2018 Dec 6;379(23):2220-2229.
11.CASPIAN: Paz-Ares L, Chen Y, et al. ESMO Open. 2022 Apr;7(2):100408.
12.ASTRUM-005: Cheng Y, Han L, et al; JAMA. 2022 Sep 27;328(12):1223-1232.
13.CAPSTONE-1: Wang J, Zhou C, Cheng Y et al; Lancet Oncol. 2022 Jun;23(6):739-747.
14.Agnese Montanino, et al. Front Oncol. 2021 May 28:11:655316.
15.EXTENTORCH: Cheng Y, et al. 2023 ESMO #LBA93.
16.Ying Cheng, et al. 2023 WCLC OA01.03
标签:


