- 此次递交是基于全球III期临床研究TROPION-Breast01,研究结果显示,德达博妥单抗在既往接受过内分泌治疗且至少一种全身系统性治疗、无法手术或转移性HR阳性、HER2阴性乳腺癌患者中的中位PFS达6.9个月,显著降低疾病进展或死亡风险达37%。
- 德达博妥单抗是一款采用独有技术设计的靶向TROP2 DXd抗体偶联药物(ADC),也是第一三共继德曲妥珠单抗后在华递交上市申请的第二款创新ADC药物。
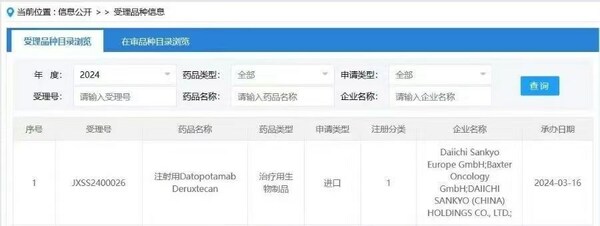
上海2024年3月16日 /美通社/ -- 中国国家药品监督管理局药品审评中心(CDE)正式受理第一三共递交的与阿斯利康联合开发和推广的靶向TROP2抗体偶联药物(ADC)德达博妥单抗(datopotamab deruxtecan,Dato-DXd)的新药上市许可申请,用于治疗既往在不可切除或转移性疾病阶段接受过系统治疗的激素体(HR)阳性、人表皮生长因子受体 2(HER2)阴性(IHC 0、IHC 1+ 或 IHC 2+/ISH-)的不可切除或转移性乳腺癌成人患者。
此次递交的德达博妥单抗的新药上市许可申请是基于关键性III期临床研究TROPION-Breast 01的数据。该研究在2023年欧洲肿瘤内科学会(ESMO)大会上公布的研究结果显示,在主要终点无进展生存期(PFS)方面,经盲态独立中心影像(BICR)评估,与研究者所选化疗(ICC)相比,德达博妥单抗用于内分泌经治的HR阳性、HER2阴性(IHC0, IHC1+或IHC2+/IHC-)转移性乳腺癌患者,可将疾病进展或死亡风险显著降低37%(风险比[HR] = 0.63;95%置信区间[CI]:0.52-0.76; p<0.0001)。德达博妥单抗治疗组的中位PFS为6.9个月,ICC为4.9个月。在不同的亚组中均观察到一致的PFS获益。此外,德达博妥单抗治疗组的客观缓解率(ORR)为36.4%,而化疗组为22.9%[1]。
在针对研究另一双主要终点总生存期(OS)的期中分析中,截至数据截止日期,德达博妥单抗也显示出优于化疗组的改善趋势(HR = 0.84;95% CI: 0.62-1.14)。研究目前正在进行中,将对OS进行进一步评估。
在安全性方面,德达博妥单抗的整体安全性良好,未发现新的安全性问题,德达博妥单抗组3级或以上治疗相关不良事件的发生率为21%,仅为化疗组的一半(化疗组为45%)。
第一三共(中国)开发总部总经理绪方恒晖博士表示:" HR阳性、HER2阴性乳腺癌是最常见的乳腺癌亚型,晚期患者在接受目前标准的内分泌治疗后仍面临较高的耐药和复发转移风险,且后续治疗选择和疗效有限。第一三共始终致力于将全球创新成果加速引入中国以填补亟待满足的治疗需求。此次德达博妥单抗上市许可申请的递交,是继德曲妥珠单抗后,我们在中国递交上市申请的第二款创新抗体偶联药物。作为同样依托于第一三共独有的DXd-ADC技术平台的产品,德达博妥单抗再次彰显了第一三共在ADC药物研发领域的强大技术实力和领导地位,相信其将成为晚期乳腺癌优选且安全的TROP2靶向ADC治疗方案。未来我们将全力推动更多创新药物在中国的研发进程以实现与全球同步可及,实现我们对中国患者的承诺。"
阿斯利康中国研发部负责人何静博士表示:"乳腺癌是中国女性中最为高发的恶性肿瘤,且近年来发病率呈不断增长态势;作为其中最主要的亚型,HR阳性、HER2阴性患者的五年生存率仅为30%,亟需创新疗法助力打破这一困境。我们感到十分欣喜能共同推动德达博妥单抗在华开发进程,这对致力于满足中国患者重大未尽之需的阿斯利康和第一三共而言都具有非凡意义,也为双方的战略合作关系增添了浓墨重彩的一笔。我们将继续密切协作,加快这一突破性疗法引进的步伐,让中国患者从中获益。"
标签: