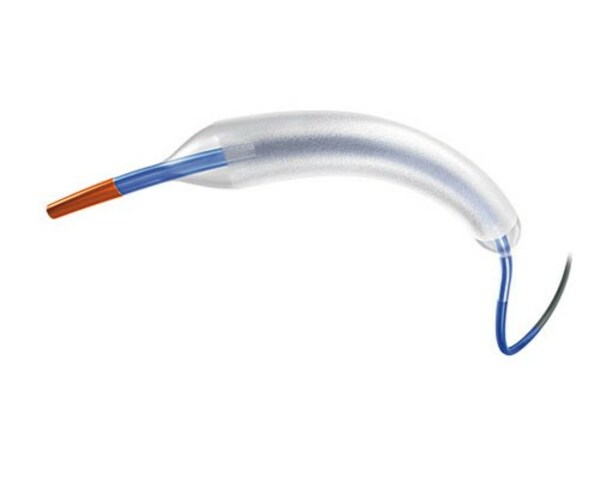
美国首个获批的冠状动脉药物涂层球囊导管,为治疗冠脉支架内再狭窄和降低复发风险提供了重要及高效的替代方案
马萨诸塞州马尔伯勒2024年3月4日 /美通社/ -- 波士顿科学公司(纽约证券交易所代码:BSX)宣布旗下AGENT™药物涂层球囊导管(DCB)已获得美国食品药品监督管理局(FDA)的批准,用于治疗冠状动脉疾病患者的支架内再狭窄(ISR)。ISR是指已植入支架的血管被斑块或疤痕组织阻塞或变窄的情况。
波士顿科学心脏介入事业部总裁Lance Bates表示:"到目前为止,全球已有超过10万名患者在临床试验和商业环境中接受过AGENT DCB治疗,我们非常高兴能够将这一经过验证的疗法引入美国市场。作为美国首个冠状动脉药物涂层球囊导管,AGENT DCB通过为具有挑战性的ISR病变提供治疗选择,解决了一个关键的未满足需求。我们期待为美国医生提供使用这种新型器械治疗患者的机会。"
虽然冠状动脉支架植入术继续显示出冠状动脉疾病患者生活质量的实质性改善,但在美国,10%的经皮冠状动脉介入治疗(PCI)手术后仍会出现ISR的问题[1,2]。作为传统治疗方法(如球囊血管成形术、额外支架层或放射疗法)的替代方案,AGENT DCB是一种紫杉醇涂层球囊导管,可将治疗剂量的药物转移到血管壁,以帮助防止ISR再次发生。
继2021年被FDA授予"突破性医疗器械"认定后,该批准得到了多中心、前瞻性、随机对照AGENT DCB研究的阳性结果的支持,该研究在美国40个中心招募了600名患者。[3]在预先指定的前480例入组患者的中期分析中,该研究在12个月时达到了靶病变失败(TLF)的主要终点,AGENT DCB在统计学上优于无涂层球囊血管成形术(17.9% vs. 28.7%,P=0.006)。[4,5]研究结果还包括:确定的/可能的支架内血栓形成为0(0.0% vs. 3.9%, P=0.001);靶血管心脏病发作风险降低49%(6.4% vs. 12.3%,P=0.03);12个月不良事件发生率低。
美国马萨诸塞州波士顿Beth Israel Deaconess医疗中心介入心脏病学主任、首席研究员Robert W. Yeh博士表示:"AGENT IDE研究证实,即使在高风险人群中,包括多层支架或患有糖尿病的患者,AGENT DCB也是冠状动脉支架内再狭窄的有效且安全的治疗选择。在美国,有限的治疗方案使得ISR治疗成为了一项难题,而这项新技术可以帮助医生在不使用放射或引入额外的金属支架层的情况下降低再狭窄的风险;对一些患者来说,放射或引入额外的金属支架层的治疗方法并不能带来满意的治疗结果。"
AGENT DCB已在欧洲、亚太地区部分国家及拉丁美洲获得批准,用于治疗ISR和先前未接受治疗的冠状动脉小血管疾病患者。未来几个月内,这款产品将在美国上市。
有关AGENT DCB的更多信息,请点击这里。
关于波士顿科学公司
波士顿科学公司承诺为生命创新。我们致力于创新医疗解决方案,改善全球患者生活。四十多年来,波士顿科学始终引领全球医疗技术行业的发展,通过提供各种广泛的高性能医疗解决方案,满足广大患者亟待解决的治疗需求,降低医疗健康成本。波士顿科学的医疗器械及相关疗法可以帮助医生诊断和治疗复杂的心血管、呼吸、消化、肿瘤、神经和泌尿系统疾病。
关于前瞻性陈述的警示性声明
本新闻稿包含美国1933年《证券法》第27A节和1934年《证券交易法》第21E节意义范畴内的前瞻性陈述。前瞻性陈述可以用诸如"预料"、"预期"、"预测"、"相信"、"计划"、"估计"、"打算"及类似的词进行标识。这些前瞻性陈述是基于我们当时可获得的信息而得出的看法、假设和估计,而非用于对未来的事件或业绩进行保证。这些前瞻性陈述包括我们对此次交易的财务和商业影响、我们的商业计划和产品性能和影响等的陈述。如果我们的基本假设被证明是错误的,或者如果某些风险或不确定性变成现实,那么实际结果可能会与我们的前瞻性陈述中所明示或所暗示的预期和预测结果存在重大差异。这些因素在某些情况下已经影响并且在未来(结合其他因素)还可能会影响我们实施业务战略的能力,并可能导致实际结果与本新闻稿中的预期结果大相径庭。因此,我们告诫读者不要过度依赖我们的任何前瞻性陈述。
可能导致这种差异的因素包括:未来经济状况、竞争状况、薪酬和监管条件;制造、分销和供应链中断及成本增加;新产品的引入;产品性能;人口发展趋势;知识产权;诉讼;金融市场情况;以及我们和竞争对手未来的商业决策。所有这些因素均难以或无法准确预测,其中许多因素我们无法控制。欲了解可能会影响我们未来业务的重要风险和不确定性因素的详细列表和描述,请参阅我们呈交美国证券交易委员会的最新10-K年度报告中的第一部分1A项"风险因素"。在已提交或之后将提交的10-Q季度报告的第二部分第1A项"风险因素"中,我们可能会更新这部分内容。我们没有意图也没有义务公开更新或修改任何前瞻性陈述以反映一些变化,这些变化可能是我们的预期改变,或是这些预期所依据的事件、条件或环境发生了改变,亦或是那些可能导致实际结果和前瞻性陈述中的结果出现差异的变化。本警示性声明适用于本文档中所有前瞻性陈述。
*该产品尚未在中国内地上市
*Robert Yeh博士是波士顿科学公司的有偿顾问。他没有得到与这篇新闻稿有关的补偿。
1. Shlofmitz E, Iantorno M, Waksman R. Restenosis of Drug-Eluting Stents: A New Classification System Based on Disease Mechanism to Guide Treatment and State-of-the-Art Review. Circ Cardiovasc Interv. 2019 Aug;12(8):e007023. doi: 10.1161/CIRCINTERVENTIONS.118.007023.
2. Moussa ID, Mohananey D, Saucedo J, et al. Trends and outcomes of restenosis after coronary stent implantation in the United States. J Am Coll Cardiol. 2020;76:1521-1531.
3. Yeh RW, Bachinsky W, Stoler R, et al. Rationale and design of a randomized study comparing the AGENT drug coated balloon to plain old balloon angioplasty in patients with In-stent restenosis. American Heart Journal. 2021;241:101-107. doi:10.1016/j.ahj.2021.07.008.
4. AGENT IDE Clinical Trial data presented at TCT 2023 by Dr. Robert Yeh.
5. TLF was defined as myocardial infarction relative to the target vessel, the need for a target lesion revascularization (TLR) procedure or cardiac mortality.
标签: